Temps de lecture : 7 minutes
Auteurs : Jennifer PINI KATZENBERGER PhD ;Mostafa SERRAR ; PhD ; Gilles GUTIERREZ D pharmacie ARTA; Tearii Te Moana ALPHA PhD ; Tim KATZENBERGER PhD ; Lama JEJO-ASLANI, Claire BALUCI.
Abstract :Les padines, phéophycées du règne des chromistes collectées sur l’île de Moorea en Polynésie française, disposent dans leur génome de grands domaines communs avec plusieurs gènes humains impliqués dans le remodelage du tissu osseux. Les régulateurs des gènes de la padine communs avec ceux des humains sont actifs sur l’expression des gènes humains malgré leur ancienneté. Cette parenté se traduit par une amélioration de la densité minérale de l’os.
La compatibilité phylogénique : un héritage commun entre végétaux et humains
D’une part, les pathologies associées au vieillissement sont plus le fait de l’altération des mécanismes de régulation que d’une modification du génome. La stabilité du génome est une des caractéristiques du vivant.
D’autre part, du fait de l’évolution, nous partageons 35% de nos gènes fonctionnels avec de nombreux végétaux. Ces gènes sont utiles aux végétaux et aux humains. De ce fait, les mécanismes de régulations comme l’activation et la répression sont identiques. Nous pouvons utiliser les molécules ou les motifs moléculaires intervenant dans le mécanisme de régulation d’un végétal pour rétablir le fonctionnement d’un gène dysfonctionnel identique chez l’homme.
Régulation biomimétique : source d’inspiration
Les molécules ou les motif moléculaires extraits du monde végétal agissant sur la régulation du fonctionnement d’un gène identique chez l’Homme. Les molécules intervenant dans une régulation identique dans deux règnes différents sont des Régulateurs Biomimétiques.
Le tissu osseux : une architecture vivante et dynamique
L’os est un tissu minéralisé composé de structures différenciant ses fonctions de soutien (vertèbres, ceintures), de protection (boîte crânienne, côtes), de flexibilité (articulation) et de mobilité (os longs). Ces structures ont des origines évolutives différentes et regroupent des cellules fortement différenciées.
La composition structurelle de l’os s’énonce par des cellules baignant dans une matrice extra cellulaire regroupant de la matière minérale et de la matière organique.
Fonctionnalités de l’os: pilier de l’organisme
L’os est un tissu minéralisé jouant plusieurs fonctions. Il contribue d’une manière évidente à notre apparence, notre stabilité et nos mouvements. Il a un rôle physiologique important avec les cellules hématopoïétiques. Enfin, il joue aussi un rôle important dans notre communication non verbale notamment dans la posture.
Les maladies ostéoarticulaires regroupent de nombreuses pathologies comme l’arthrose, l’ostéoporose et les rhumatismes inflammatoires chroniques (polyarthrite rhumatoïde, spondylarthrite ankylosante, arthrite chronique juvénile, rhumatisme psoriasique). Sur le plan légal, ces maladies s’inscrivent dans les actes médicaux pour leur diagnostic et leur traitement. Dans l’antiquité grecque, toute la santé de notre squelette avait sa théophanie : Hygié, Panacée, Machaon, Meditrine, Asceso… Aujourd’hui, les cliniciens disposent d’une large gamme de soins pour soigner les maladies ostéoarticulaires. Depuis la nutrition symbolisé par Ascéso (Diétée) fille d’Asclépios[2] avec des apports en calcium, magnésium, vitamine D etc, jusqu’à la chirurgie figuré par Machaon fils ainé d’Asclépios. Il appartient au clinicien et aux thérapeutes de proposer les soins convenant le mieux (index thérapeutique) au patient. Le patient choisit le thérapeute et les soins qui lui conviennent.
Parmi les maladies de l’os, l’ostéoporose est une pathologie systémique du squelette caractérisée par une diminution de la densité minérale osseuse (DMO BMP en UK) et une altération de la microarchitecture osseuse, entraînant une fragilité accrue avec une augmentation du risque de fracture. Selon la International Osteoporosis Foundation, environ 200 millions de femmes dans le monde sont touchées par l’ostéoporose, et près d’une femme sur trois de plus de 50 ans présentera une fracture ostéoporotique au cours de sa vie. Il faut ajouter que les hommes perdent leur masse minérale osseuse à la même vitesse que les femmes. Partant d’une masse d’os plus importante, le risque fracturaire est retardé.
En France, les données actualisées 2024 et 2025 de Santé Publique France et du Inserm estiment qu’environ 3,5 à 4 millions de personnes sont concernées par l’ostéoporose, dont près de 2,5 à 3 millions de femmes. Après 65 ans, environ 35 à 40 % des femmes présentent un risque élevé de fracture ostéoporotique, en particulier au niveau du col fémoral, desvertèbres et du poignet. En France, chaque année, on estime à plus de 370 000 le nombre de fractures de fragilité.
L’augmentation de l’espérance de vie et le vieillissement démographique accentuent l’impact socio-économique de cette pathologie, notamment en raison des fractures ostéoporotiques (rachis, hanche, poignet).
[1] Le terme de collagène (qui génère de la colle) vient de l’extraction de la colle en faisant bouillir les os de poissons ou de mammifères. Il existe une trentaine de types de collagène. Apparus dans la composition des êtres vivant il y a quelque 800 millions d’années.
[2] Dieu de la médecine chez les grecques remplacé par Esculape dans le panthéon des romains
Sur le plan physiopathologique, l’ostéoporose résulte d’un déséquilibre du remodelage osseux. Ce remodelage est constant au cour de la vie. Il est caractérisé par la construction du tissu par des ostéoblastes et une résorption par les ostéoclastes. Si la résorption ostéoclastique physiologique dépasse les capacités de construction des ostéoblastes, elle devient excessive au même titre qu’une activité ostéoblastique insuffisante. Cette formulation montre que l’ostéoporose s’appuie sur une description anatomique et regroupe des dysfonctionnements très différents qu’il faudra traiter de manière différente. Les déficits en calcium et en vitamine D et K, sont quelques-unes des carences[3] dues au vieillissement comme celles des hormones qui scandent la ménopause et le vieillissement cellulaire. L’inflammation chronique constitue aussi l’un les facteurs déterminants.
L’ostéoporose est la conséquence de l’aggravation de la perte calcique physiologique liée à l’âge. Cette perte physiologique devenant excessive, elle fait le lit de la maladie ostéoporotique. Elles se définie par :
Une activité excessive des ostéoclastes ou une insuffisance de l’activité ostéoblastique entraîne une perte progressive du capital osseux. L’ostéopénie constitue un stade intermédiaire entre os normal et ostéoporose.
Les principaux facteurs de risque incluent
Les stratégies de prévention reposent sur une approche multimodale incluant l’activité physique régulière : exercices en charge et renforcement musculaire, un apport nutritionnel adéquat en calcium, vitamine D et K, entrainement à la chute, ainsi que la réduction des facteurs de risque comme le tabagisme, la sédentarité et l’alcool. L’activité physique doit être différenciée de la pratique sportive[4],. Les recommandations actualisées 2023-2024 insistent également sur le dépistage ciblé par ostéodensitométrie (DXA) chez les populations à risque.
[3] Il ne s’agit pas uniquement de carences nutritionnelles. La réduction de la mobilité, la diminution émotionnelle, la réduction de l’adaptation des organes hématopoïétiques
[4] L’activité physique se caractérise par une augmentation de la fréquence cardiaque, de la PCO², une température stable et un rapide retour aux valeurs normales. La pratique sportive montre une élévation de la température corporelle, un pouls dépassant le seuil adaptatif, une PCO² fortement augmentée et une pression artérielle augmentée associés à une augmentation de HSPs. Le retour à la valeur physiologique peut prendre plusieurs heures. Cette pratique requière un entrainement bien encadré pour éviter la création et l’accumulation de lésions.
Sur le plan physiopathologique, l’ostéoporose résulte d’un déséquilibre du remodelage osseux. Ce remodelage est constant au cour de la vie. Il est caractérisé par la construction du tissu par des ostéoblastes et une résorption par les ostéoclastes. Si la résorption ostéoclastique physiologique dépasse les capacités de construction des ostéoblastes, elle devient excessive au même titre qu’une activité ostéoblastique insuffisante. Cette formulation montre que l’ostéoporose s’appuie sur une description anatomique et regroupe des dysfonctionnements très différents qu’il faudra traiter de manière différente. Les déficits en calcium et en vitamine D et K, sont quelques-unes des carences[3] dues au vieillissement comme celles des hormones qui scandent la ménopause et le vieillissement cellulaire. L’inflammation chronique constitue aussi l’un les facteurs déterminants.
L’ostéoporose est la conséquence de l’aggravation de la perte calcique physiologique liée à l’âge. Cette perte physiologique devenant excessive, elle fait le lit de la maladie ostéoporotique. Elles se définie par :
Une activité excessive des ostéoclastes ou une insuffisance de l’activité ostéoblastique entraîne une perte progressive du capital osseux. L’ostéopénie constitue un stade intermédiaire entre os normal et ostéoporose.
Les principaux facteurs de risque incluent
Les stratégies de prévention reposent sur une approche multimodale incluant l’activité physique régulière : exercices en charge et renforcement musculaire, un apport nutritionnel adéquat en calcium, vitamine D et K, entrainement à la chute, ainsi que la réduction des facteurs de risque comme le tabagisme, la sédentarité et l’alcool. L’activité physique doit être différenciée de la pratique sportive[4],. Les recommandations actualisées 2023-2024 insistent également sur le dépistage ciblé par ostéodensitométrie (DXA) chez les populations à risque.
[3] Il ne s’agit pas uniquement de carences nutritionnelles. La réduction de la mobilité, la diminution émotionnelle, la réduction de l’adaptation des organes hématopoïétiques
[4] L’activité physique se caractérise par une augmentation de la fréquence cardiaque, de la PCO², une température stable et un rapide retour aux valeurs normales. La pratique sportive montre une élévation de la température corporelle, un pouls dépassant le seuil adaptatif, une PCO² fortement augmentée et une pression artérielle augmentée associés à une augmentation de HSPs. Le retour à la valeur physiologique peut prendre plusieurs heures. Cette pratique requière un entrainement bien encadré pour éviter la création et l’accumulation de lésions.
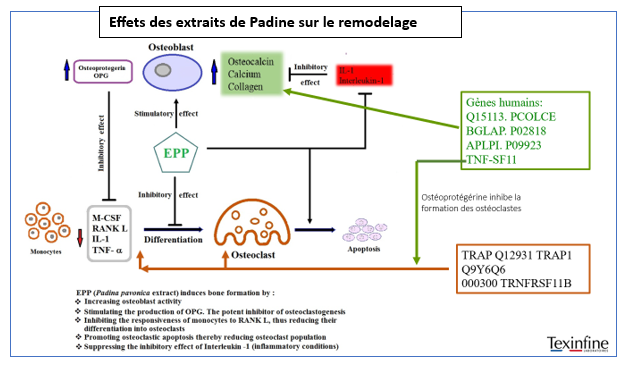
L’intérêt des ressources marines dans la prévention et santé osseuse découvert par le Pharmacien Gilles GUTIERREZ suscite un intérêt croissant. Certaines algues ou Phaeophyceae, notamment Padina pavonica, contiennent une dizaine de gènes communs avec les Hommes concernant le remodelage osseux.
Padina pavonica ou algue brune (Phéophycée) à cornets blancs ou encore appelée « Queue de Paon » appartient à la famille des Dictyotaceae. Sa morphologie est surprenante car c’est un des rares végétaux à ne pas présenter de bilatéralisation[5]. Sa « queue de paon » correspondant à des thalles blanchis par des dépôts d’aragonite (minéral de la nacre) concentriques lui confère une spécificité biologique unique. Elle est revêtue de cristaux orthorhombiques de carbonate de calcium sur ses frondes à un taux le plus élevé de toutes les algues (jusqu’à 240 g/m-2/an-1). Ainsi, on l’appelle algue «calcifiante» ou algue calcifiée. Cette algue brune dispose donc d’un mécanisme ingénieux capable de réguler la fixation du calcium sur la surface de ses frondes. Étant composée d’un exosquelette calcifié, la Padina pavonica est capable de maintenir la fonction des cellules osseuses en restructurant la matrice extracellulaire. Cette capacité naturelle de calcification suggère un intérêt biomimétique potentiel dans la régulation du métabolisme calcique.
Des études en cliniques observationnelles suggèrent un effet potentiel sur la stimulation des gènes impliquées dans l’activité ostéoblastique et la modulation de la résorption osseuse. Une étude génomique comparative entre le génome humain et celui de la Padine révèle l’existence de séquences génomiques communes (ou contigs) entre le genre « Homo » et la Padine de Tahiti. Une étude plus approfondie du pourcentage de conservation des régions ou séquences des domaines a révélée qu’il existait des suites de plus de 300 bases nucléosidiques. Sur la base d’un minimum de 50 acides nucléiques consécutifs, plus de 30 gènes ont été notés présentant de très hautes analogies entre le génome de la Padine et le génome humain.
Parmi les gènes présents dans le génome de la Padine, on notera notamment les gènes qui interviennent à deux niveaux majeurs du remodelage osseux : formation et la résorption osseuses, constituant un noyau fonctionnel central dans la régulation de cet l’équilibre.
La formation osseuse, assurée par les ostéoblastes, implique notamment les gènes TNFRSF11B (Ostéoprotégérine, OPG), ALPL (Phosphatase alcaline, isoforme tissulaire non spécifique) et BGLAP (Ostéocalcine), qui interviennent respectivement dans la régulation de l’axe RANK/RANKL, la minéralisation de la matrice et la production d’ostéocalcine, marqueur de différenciation ostéoblastique.
La voie RHOA joue un rôle central dans le remodelage osseux, en particulier dans la fonction des ostéoclastes. Les gènes RHOA (Ras homolog family member A. Petite protéine GTPase impliquée dans l’organisation du cytosquelette d’actine), ROCK1 (Rho-associated coiled-coil containing protein kinase1, Kinase activée par RHOA), PPP1R12A (MYPT1, Protein phosphatase 1 regulatory subunit 12A Sous-unité régulatrice de la myosine phosphatase) et ECT2 (Epithelial cell transforming sequence 2, Facteur d’échange de nucléotides activant RHOA) participent à l’organisation du cytosquelette d’actine, essentielle à la formation de l’anneau d’actine et de la bordure en brosse nécessaires à la résorption osseuse. Cette voie intervient également dans la migration et la différenciation cellulaire, des processus clés du remodelage osseux.
Par ailleurs, les gènes suivants ont été identifiés comme présents dans la Padine et impliqués dans le remodelage osseux : PCOLCE (Procollagen C-endopeptidase enhancer), TNFSF11 (RANKL), ALPP (Phosphatase alcaline placentaire), ALPPL2 (Alkaline phosphatase placental-like 2), TRAP1 et TNFRSF11A (RANK). Ces gènes sont classiquement associés à la régulation de la formation et de la résorption osseuses, notamment via l’axe RANK/RANKL/OPG et les marqueurs de différenciation ostéoblastique et ostéoclastique.
D’autres gènes contribuant de manière plus indirecte au remodelage en régulant la prolifération et la division cellulaire ont été identifiés dans le génome de la Padine. Il s’agit de AURKB, BIRC5 (Survivin), KIF23, KIF4A, PRC1 et INCENP, qui interviennent principalement dans la mitose des précurseurs ostéoblastiques et ostéoclastiques. Leur rôle se concerne donc sur le renouvellement cellulaire.
Les gènes MYH11, MYH7 et SEPT1, aussi identifiés dans le génome de la Padine, sont impliqués dans l’organisation du cytosquelette et la contractilité cellulaire. Leur implication dans le remodelage osseux est plus indirecte, via la régulation de la dynamique cellulaire.
Les gènes MYH11, MYH7 et SEPT1, aussi identifiés dans le génome de la Padine, sont impliqués dans l’organisation du cytosquelette et la contractilité cellulaire. Leur implication dans le remodelage osseux est plus indirecte, via la régulation de la dynamique cellulaire.
[3] Il ne s’agit pas uniquement de carences nutritionnelles. La réduction de la mobilité, la diminution émotionnelle, la réduction de l’adaptation des organes hématopoïétiques
[4] L’activité physique se caractérise par une augmentation de la fréquence cardiaque, de la PCO², une température stable et un rapide retour aux valeurs normales. La pratique sportive montre une élévation de la température corporelle, un pouls dépassant le seuil adaptatif, une PCO² fortement augmentée et une pression artérielle augmentée associés à une augmentation de HSPs. Le retour à la valeur physiologique peut prendre plusieurs heures. Cette pratique requière un entrainement bien encadré pour éviter la création et l’accumulation de lésions.
La répétition des gènes chez les végétaux et le ratio des gènes codant par rapport à la totalité de l’ADN sont une indication sur l’ancienneté de l’évolution. Les séquences conservées correspondent à des séquences identiques d’acides nucléiques entre les deux espèces sur un domaine de leur génome. Il s’agit de séquences orthologues. La haute conservation indique que ces séquences ont été maintenues au cours de l’évolution pendant environ 600 millions d’années.
Au fils du temps, ces séquences d’acides nucléiques du génome auraient pu évoluer par recombinaison ou par suppression en raison des mutations et des délétions aléatoires ou encore des réarrangements chromosomiques mais leur utilité dans deux règnes a préservé ces domaines génomiques. Il est à noter que la conservation peut se faire dans les séquences d’acides nucléiques codantes et non codantes, de même les séquences d’ADN conservées peuvent avoir une valeur fonctionnelle ou structurelle.
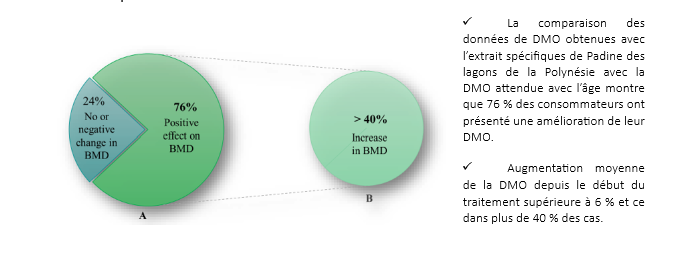
L’utilisation d’extraits de Padines de Polynésie permet d’observer une augmentation de la DMO chez plus de 76% des consommateurs.
Références scientifiques
Apparition du collagène : Guillaume Lecointre, « Héritages adaptatifs », dans Petit traité d’anatomie superflue. L’évolution à travers notre corps, Delachaux et Niestlé, septembre 2024, 240 p. (ISBN978-2-603-03043-1), p. 25 https://isyeb.mnhn.fr/fr/actualites/petit-traite-danatomie-superflue-levolution-travers-notre-corps-9634.
Cadar, E.; Popescu, A.; Dragan, A.-M.-L.; Pesterau, A.-M.; Pascale, C.; Anuta, V.; Prasacu, I.; Velescu, B.S.; Tomescu, C.L.; Bogdan-Andreescu, C.F.; et al. Bioactive Compounds of Marine Algae and Their Potential Health and Nutraceutical Applications: A Review. Drugs2025, 23, 152. https://doi.org/10.3390/md23040152. Currently, marine algae are still an under-exploited natural bioresource of bioactive compounds. Seaweeds represent a sustainable source for obtaining bioactive compounds that can be useful for the fabrication of new active products with biomedical benefits and applications as biomedicinals and nutraceuticals. The objective of this review is to highlight scientific papers that identify biocompounds from marine macroalgae and emphasize their benefits. The method used was data analysis to systematize information to identify biocompounds and their various benefits in pharmaceuticals, cosmetics, and nutraceuticals. The research results demonstrate the multiple uses of seaweeds. As pharmaceuticals, seaweeds are rich sources of bioactive compounds like polysaccharides, protein compounds, pigments, and polyphenols, which have demonstrated various pharmacological activities such as antioxidant, antibacterial, anti-inflammatory, antiviral, anticoagulant, and potentially anticarcinogenic effects. Seaweed has gained recognition as a functional food and offers a unique set of compounds that promote body health, including vitamins, minerals, and antioxidants. In conclusion, the importance of this review is to expand the possibilities for utilizing natural resources by broadening the areas of research for human health and marine nutraceuticals.
Compston J, McClung M, Leslie W. Osteoporosis. The Lancet. Mise à jour clinique continue 2023-2024. https://pubmed.ncbi.nlm.nih.gov/30696576/ Fractures resulting from osteoporosis become increasingly common in women after age 55 years and men after age 65 years, resulting in substantial bone-associated morbidities, and increased mortality and health-care costs. Research advances have led to a more accurate assessment of fracture risk and have increased the range of therapeutic options available to prevent fractures. Fracture risk algorithms that combine clinical risk factors and bone mineral density are now widely used in clinical practice to target high-risk individuals for treatment. The discovery of key pathways regulating bone resorption and formation has identified new approaches to treatment with distinctive mechanisms of action. Osteoporosis is a chronic condition and long-term, sometimes lifelong, management is required. In individuals at high risk of fracture, the benefit versus risk profile is likely to be favourable for up to 10 years of treatment with bisphosphonates or denosumab. In people at a very high or imminent risk of fracture, therapy with teriparatide or abaloparatide should be considered; however, since treatment duration with these drugs is restricted to 18-24 months, treatment should be continued with an antiresorptive drug. Individuals at high risk of fractures do not receive adequate treatment and strategies to address this treatment gap-eg, widespread implementation of Fracture Liaison Services and improvement of adherence to therapy-are important challenges for the future.
International Osteoporosis Foundation. Osteoporosis facts and statistics 2024 update. IOF, 2024. https://www.osteoporosis.foundation/
Ostéoporose : données épidémiologiques actualisées, dossier thématique 2023-2024. https://www.inserm.fr/dossier/osteoporose/
Kanis JA et al. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. https://pmc.ncbi.nlm.nih.gov/articles/PMC7026233/
Santé Publique France. Fractures de fragilité et hospitalisations associées en France, rapport 2024. https://www.santepubliquefrance.fr/maladies-et-traumatismes/traumatismes/chute/documents/bulletin-national/hospitalisations-et-mortalite-en-lien-avec-une-chute-chez-les-personnes-de-65-ans-et-plus-en-france.-donnees-2015-2024
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité

