Phytothérapie et Galénique : Pourquoi un extrait actif est plus efficace ?
Temps de lecture : 5 Minutes
Phytothérapie et Galénique : Pourquoi un extrait actif est plus efficace ?
I. L’origine de la Phytothérapie
Depuis toujours, l’être humain s’est intéressé aux plantes, que ce soit pour se nourrir, chasser ou se soigner, comme peuvent en témoigner des vestiges archéologiques tombes, peintures rupestres, poteries. Cependant, c’est avec l’apparition de l’écriture que les usages médicinaux sont précisés et sont documentés. Les premières traces écrites remontent à 5000 av. J.-C. avec la tablette sumérienne de Nippur, mentionnant plus de 250 plantes, dont le pavot.
En Chine, le “Shennong bencao jing” (2500 av. J.-C.) est considéré comme un des premiers traités médicaux. D’autres textes anciens, comme le papyrus d’Ebers (1500 av. J.-C.) en Égypte ou les Védas en Inde, témoignent également de l’usage ancien et structuré des plantes médicinales.
On distingue 3 grandes périodes de l’Histoire de la phytothérapie :
L’Antiquité
En Grèce et dans d’autres civilisations, des figures clés comme Hippocrate (recensement de plus de 380 plantes), Théophraste (≈ 500 plantes, premières expérimentations de toxicité) et Aristote (concept du totum des plantes) ont marqués l’usage systématique des plantes. D’autres auteurs romains/grecs comme Dioscoride, Pline l’Ancien ou Galien ont poursuivis cette tradition.
Dans son livre « Histoire naturelle », publié vers 77, Pline l’Ancien évoquait déjà les vertus de la fleur de sel (Flos salis) et de sa dissolution (extraction) dans le vin et l’eau: « Cette fleur de sel produit une sorte d’huile aussi surprenant que cela puisse paraître (Optimo ex eo, quod olei quamdam pinguitudinem reddit. Est enim etiam in sale pinguitudo, quod miremu). Il y a de la graisse même dans le sel ! » S’exclame-t-il. Pline l’Ancien ajoute qu’elle n’a pas de pouvoir nutritif mais qu’elle est relâchante, (décontractante), stimulante et pouvant porter remède à la lassitude (psychostimulante) « solvit in vino et aqua, acopis et smegmatis utilis » (Volume 31 de 37 volumes, chapitre XLII).
Le Moyen Âge
En Europe, les moines et l’Église ont transmis la connaissance des « simples » dites plantes « médicinales » (par ex. Hildegarde de Bingen). Dans le monde islamique ou persan, des médecins comme Avicenne ou Ibn al‑Baytār ont constitué de vastes traités sur les plantes (1 400 espèces pour Ibn al‑Baytār).
Les Temps modernes jusqu’à aujourd’hui
L’exploration et la colonisation a ouvert la voie à la découverte de nombreuses plantes exotiques comme la quinquina, le curcuma, ou encore la vanille. La chimie moderne nous permet désormais d’isoler les principes actifs et surtout de synthétiser des molécules comme l’acide salicylique précurseur de l’aspirine en 1899. Entre 1981 et 2014, environ 42 % des molécules de médicaments commercialisés sont directement tirées de la nature dont 25 % sont inspirées de structures naturelles.
A noter que la phytothérapie n’est pas propre à l’espèce humaine. De nombreuses espèces animales, savent choisir dans leur habitat les plantes utiles pour corriger des carences alimentaires ou soigner certaines maladies. On parle de zoopharmacognosie, une branche de l’éthologie animale et de la pharmacologie qui étudie le comportement d’auto-médication propre à certains animaux.
II. Définition de la phytothérapie
Le terme de phytothérapie vient du grec phyton qui signifie plantes et therapeia qui signifie soigner. Elle est considérée par l’Organisation mondiale de la santé (OMS) comme une médecine conventionnelle. Elle repose sur un traitement thérapeutique à base de plantes. Il existe une distinction entre la phytothérapie traditionnelle et la phytothérapie moderne, ou « phytothérapie médicale ».
La phytothérapie traditionnelle est basée sur l’expérience et l’observation et une approche holistique pour laquelle les effets des plantes sont considérés dans leur globalité. Elle est fondée sur une utilisation directe de la poudre de plantes ou de leurs préparations sous forme de tisanes ou de d’infusions.
La phytothérapie moderne, utilise des méthodes modernes d’extraction et de purification des principes actifs contenus dans les plantes, et valide leurs propriétés bénéfiques pour la santé par une approche scientifique d’analyses biochimiques et pharmacologiques appuyées parfois par des études observationnelles voir même des essais cliniques.
Le principe actif : clef de voute du remède.
1) Les nutriments
Les vitamines hydrosolubles, les sels minéraux sont absorbés tels qu’ils sont. Les protéines et les sucres complexes sont digérés avant d’être assimilés. Certains substances ne sont pas digestes mais représentent un intérêt comme la cellulose et la chitine des champignons. Si la cellulose peut fermenter dans le tube digestif, la chitine (paroi des champignons) transitera intacte dans les fèces.
2) Les molécules actives
a) Certaines molécules comme les alcaloïdes n’ont pas de rôle identifié pour la plante.
b) Il existe des molécules d’intérêt différents pour la plante et pour les humains, par exemple l’acide salicylique joue un rôle chez le végétal dans la défense et l’identification des espèces. Chez l’homme, il agît au niveau des signaux de l’inflammation et des plaquettes.
c) Il existe des molécules d’intérêt similaire pour la plante et pour les humains. En fait cela relève des parentés (cladistiques) due à l’évolution. Dans ce cas particulier, la plante ne disposant pas d’une circulation aussi efficace que les animaux, la plante disposera de palettes de molécule activatrice et frénatrice d’un métabolisme. Pour en recueillir l’activité des procédures de séparation devront être mises en œuvre.
Qu’est-ce que la galénique ?
La galénique (ou pharmacie galénique) est la science des mises en formes pharmaceutiques, l’art de transformer substances actives ici les plantes médicinales, en formes utilisables et efficaces. Elle étudie la transformation d’un principe actif (issu d’une plante, d’un minéral ou d’une molécule chimique) en une forme utilisable, stable, efficace, et acceptable par le patient (infusions, pilules, comprimés, cachets, pommades, crème etc.).
La mise en forme galénique des produits à base de plantes existe depuis au moins 5000 ans, avec une évolution constante des formes et des techniques. Il est probable que les première plantes ont été consommées fraîche et crus. Puis le séchage et la réhydratation par infusion, macération. Elle devient progressivement plus raffinée avec l’apparition très rapide de la diversification des solvants ajoutant à l’eau, le lait, le vin, le vinaigre et l’alcool. Cela n’a pas cessé d’évoluer depuis l’Antiquité, en passant par la médecine arabo-musulmane médiévale, persane et chinoise jusqu’à former les bases de la pharmacie moderne.
La galénique des produits issus des plantes est donc, sans conteste, l’une des plus riches et variées. Certains végétaux présentaient un goût ou une odeur si désagréables qu’ils étaient difficilement consommables tels quels. Pour en faciliter la prise, les premiers thérapeutes ont donc eu l’idée de mélanger les poudres de plantes avec du miel et de la farine, donnant ainsi naissance aux premières pilules. Si cette préparation permettait de masquer efficacement le goût, elle restait insuffisante pour neutraliser les odeurs. Afin d’y remédier, on recouvrait alors ces pilules d’une fine couche de cire, voire d’un film d’or, pour mieux isoler l’odeur et améliorer leur acceptabilité. D’où l’expression, dorer la pilule.
Si la phytothérapie fournit le contenu actif, la galénique elle détermine comment l’administrer (forme, dose, support).
III. Quel est l’intérêt d’un extrait actif par rapport à la poudre de plante ?
Deux principaux avantages de la phytothérapie moderne
1/ Efficacité
Dans la phytothérapie traditionnelle, la plante ou partie de la plante (feuille, racine, fruit,…) sera utilisée en totalité. En effet, même si une poudre de plante contient une partie spécifique de la plante broyée, elle ne fera pas de distinction entre les composants actifs et inactifs. Les principes actifs contenus dans cette poudre seront donc dilués parmi d’autres composants inactifs ou peu actifs. Si une tisane est une forme d’extraction à l’eau chaude, seuls les composants solubles dans l’eau seront extrait et souvent à très faibles doses.
En phytothérapie moderne, un extrait actif est obtenu en sélectionnant et concentrant les molécules responsables de l’effet thérapeutique (alcaloïdes, flavonoïdes, polyphénols, saponines, etc.). Un extrait sera donc plus concentré en molécules actives et donc plus efficaces par rapport à une poudre de plante.
Un des principaux avantages des extraits actifs de plantes est leur contrôle précis de la qualité et de l’efficacité. Contrairement à la poudre de plante entière ou à une infusion, les extraits actifs peuvent être standardisés : cela signifie que chaque dose contient une quantité constante et garantie de principes actifs, c’est-à-dire les molécules responsables de l’effet thérapeutique recherché (par exemple : curcuminoïdes dans le curcuma, ginsénosides dans le ginseng, etc.).
a) la standardisation moléculaire. Cette standardisation est possible car l’extrait est obtenu par un processus d’extraction et de purification contrôlé, qui isole les composés d’intérêt et élimine les parties inactives ou moins utiles de la plante. Ainsi, il est possible de garantir l’efficacité d’un produit ou chaque comprimé contient exactement le même dosage en actifs, quel que soit le lot de production. C’est le cas des formes contenant du séné où la teneur en sénosides est garantie.
b) L’activité peut être mesuré non pas avec une molécule mais par son activité ou sa correspondance par rapport à un étalon. C’est le cas de la molécules de vitamine D3, de certains antibiotiques, des motifs moléculaires complexes comme l’héparine. C’est le cas des produits extraits de plante présentés par les Laboratoire ICP-TEXINFINE.
En phytothérapie traditionnelle, de fortes variations rendent la teneur en actifs incertaine dans les préparations non standardisées. En effet, les conditions de culture (climat, ensoleillement,..), période de récolte, la partie de la plante utilisée ou encore les méthodes de séchage et de stockage sont autant de facteurs qui entrainent une irrégularité et donc limite l’efficacité thérapeutique des plantes non « standardisées ». C’est-à-dire n’ayant pas suivi des processus d’extraction de purification et/ou de fractionnement établissant une référence d’activité par rapport à un « standard ».
2/ Biodisponibilité
Un autre avantage essentiel des extraits actifs réside dans leur meilleure assimilation par l’organisme, c’est-à-dire leur biodisponibilité. Certains principes actifs présents dans les plantes sont mal absorbés sous leur forme brute (poudre ou tisane), soit parce qu’ils sont :
- Peu solubles dans l’eau (donc peu extraits dans une macération, une décoction, infusion),
- Mal absorbés par l’intestin sans adjuvants ou par la présence de substance absorbante comme certaines cellulose, le chitosane, la paraffine, certaines silices organiques.
- Rapidement métabolisés ou éliminés.
C’est le cas, par exemple, de la curcumine, principe actif du curcuma, qui a une très faible biodisponibilité naturelle. Des extraits améliorés (avec pipérine, phytosomes, ou encapsulation dans des phospholipides) permettent d’améliorer l’absorption par l’organisme.
Autre exemple, la Figue de Barbarie, plante des zones arides tropicales, riche en vitamine E, en acides gras essentiels (dans l’huile de graines), ainsi qu’en bétalaïnes, des pigments aux propriétés anti-inflammatoires et protectrices. En forme brute (poudre, jus ou macération), les composés actifs sont peu biodisponibles, peu solubles dans l’eau, sensibles à l’oxydation et instables à l’air et la lumière. Mais en forme galénique optimisée (extrait actif ou extraits titrés en bétalaïnes ou sous forme micronisée), les molécules actives sont mieux préservées et stabilisées pour une optimisation de l’efficacité thérapeutique.
Les avantages des produits TEXINFINE : La phytothérapie moderne
La phytothérapie selon TEXINFINE est basée sur des méthodes spécifiques d’extraction et de purification des régulateurs biomimétiques® contenus dans les plantes. Ces méthodes d’extraction rendent possible la mesure de l’activité biologique et pharmacologique. Elles permettent d’utiliser les régulateurs de gènes ciblés dans une plante pour un objectif de santé humaine précis.
L’isolement des régulateurs présents chez le végétal est une nécessité pour garantir l’activité chez l’humain. Le système vasculaire des végétaux est peu efficace. Ils disposent d’une palette de molécules pour répondre à l’ensemble des sollicitations environnementales. Dans un extrait de plantes, pour une même activité biologique, il y aura autant de promoteurs que de répresseurs. Il faut donc séparer les régulateurs « activateurs » des régulateurs « inhibiteurs » par purification ou fractionnement.
Références
- Balick, M. J., & Cox, P. A. (1996). Plants, People, and Culture: The Science of Ethnobotany. New York: Scientific American Library.
- Dalby, A. (2003). Food in the Ancient World from A to Z. Routledge.
- Nunn, J. F. (2002). Ancient Egyptian Medicine. University of Oklahoma Press.
- Pliny the Elder. (77 AD). Naturalis Historia.
- Newman, A. (1991). The Formative Age of Islamic Medicine. Edinburgh University Press.
- Sneader, W. (2000). Drug Discovery: A History. John Wiley & Sons. (PDF) Drug Discovery: A History (Sneader, Walter)
- Newman, D. J., & Cragg, G. M. (2016). Natural Products as Sources of New Drugs from 1981 to 2014. Journal of Natural Products, 79(3), 629–661.
- World Health Organization (WHO). (2004). WHO Global Report on Traditional and Complementary Medicine 2019.
- Fabricant, D. S., & Farnsworth, N. R. (2001). The Value of Plants Used in Traditional Medicine for Drug Discovery. Environmental Health Perspectives, 109(Suppl 1), 69–75.
- McCance, R. A., & Widdowson, E. M. (2002). The Composition of Foods, 6th Edition. Royal Society of Chemistry.
- Harborne, J. B. (1998). Phytochemical Methods: A Guide to Modern Techniques of Plant Analysis. Chapman & Hall. Dubick MA (1986). Historical perspectives on the use of herbal preparations to promote health. J Nutr.
- Blumenthal, M., et al. (2000). Herbal Medicine: Expanded Commission E Monographs. American Botanical Council.
- Tabanelli R, Brogi S, Calderone V. (2021). Improving Curcumin Bioavailability: Current Strategies and Future Perspectives. Pharmaceutics.
- Gentile C, Tesoriere L, Allegra M, Livrea MA, D’Alessio P. (2004). Antioxidant betalains from cactus pear (Opuntia ficus-indica) inhibit endothelial ICAM-1 expression. Ann N Y Acad Sci.
Ces sujets vous intéressent ?
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité
Ces articles pourraient vous intéresser

Les chaperonnes, ces protéines indispensables hautement conservées
Temps de lecture : 9 minutes
Les chaperonnes, ces protéines indispensables hautement conservées
L’ADN et l’ensemble des gènes qu’il contient codent uniquement pour des protéines. Tout ce qui est inscrit dans l’ADN est transcrit par l’ARN polymérase en ARN messager, puis traduit par les ribosomes en une chaîne d’acides aminés, formant ainsi une protéine non encore conformée. Considérées comme le troisième maillon de la chaîne d’expression du code génétique, les protéines sont indispensables à la structure et au bon fonctionnement de nos cellules. Ces protéines n’acquièrent leur fonctionnalité qu’en adoptant un repliement tridimensionnel précis. Une altération de cette structure entraîne une perte de fonction ou des agrégations pathologiques, d’où l’importance des protéines chaperonnes, comme les HSPs, qui assurent le maintien et la correction du bon repliement.
Les chaperonnes, protéines de choc HSPs (Heat Shock Proteins) sont des protéines qui permettent à nos cellules de lutter contre le stress cellulaire et jouent aussi un rôle dans les défenses de l’organisme en préservant la forme tridimensionnelle des protéines et en éliminant les protéines irrémédiablement endommagées.
L’origine d’un stress cellulaire, situation dans laquelle une cellule est exposée à des conditions défavorables sublétals menaçant son équilibre interne (homéostasie), est variée. Elle peut être nutritionnelle, biochimique, bactériologique, virale, thermique, ou encore environnementale et altère le repliement des protéines et en cela les fonctions cellulaires.
En conséquence de ce stress, les protéines, modifient leur forme tridimensionnelle et en conséquence, altèrent leur fonction. Les processus cellulaires se trouvent entravés ou simplement ralenti ce qui provoque une accumulation de stress par l’accroissement des radicaux libres, des déchets cellulaires et de facteurs complétant le stress. Ce cercle vicieux accentue le stress cellulaire et épuise progressivement la capacité des cellules à maintenir le bon fonctionnement de leurs processus vitaux.
Pour tenter de rétablir son équilibre, la cellule active divers mécanismes de protection et de réparation, tels que l’induction des protéines de choc thermique, les systèmes antioxydants, la réparation de l’ADN ou encore l’autophagie. Son objectif sera de restaurer l’homéostasie et d’assurer sa survie. Toutefois, si les dommages dépassent les capacités d’adaptation par restauration de la conformation ou élimination des protéines trop endommagées, la cellule entrera en apoptose (mort programmée par disparition du noyau mais persistance des fonctionnalités du cytoplasme).
Le mécanisme cellulaire d’induction des protéines de choc thermique est commun à presque tous les organismes, des bactéries aux champignons, en passant par les plantes et les animaux, y compris les êtres humains et est donc hautement conservé au cours de l’évolution.
Les HSPs jouent un rôle crucial dans le maintien du fonctionnement de l’intégrité cellulaire. Elles évitent les interactions moléculaires indésirables et favorisent celles qui sont souhaitables.
La découverte des HSPs date de 1962, à l’Institut de génétique de Pavie, en Italie, lorsque quelqu’un augmenta par inadvertance la température d’un incubateur contenant des drosophiles. Lorsque le généticien Ferruccio Ritossa examina les cellules des insectes ayant subi un tel « choc thermique », il remarqua que leurs chromosomes avaient enflé par endroits : des gènes avaient été activés dans ces régions et des protéines synthétisées. Des protéines, nommés Heat Shock Proteins HSPs, ont donc été produites en réponse à une condition stressante afin d’éviter toute dénaturation et garantir la bonne conformation des protéines dans la cellule.
Les différentes familles d’HSPs
Les protéines de choc thermique (HSPs) sont classées et désignées selon leur localisation cellulaire, leur mode d’expression et surtout leur poids moléculaire. Ainsi, les familles Hsp60, Hsp70 et Hsp90, parmi les plus étudiées, correspondent respectivement à des protéines d’environ 60, 70 et 90 kDa (kilo-Dalton où 1 kDa est environ égal à 1 000g/mole).
Une petite protéine de 8 kDa, l’ubiquitine, impliquée dans le marquage des protéines destinées à la dégradation, présente également des caractéristiques typiques des protéines de choc thermique. Ce type de petites HSPs contiennent parfois un domaine de liaison aux protéines, dit « alpha-crystalline », constitué d’environ 80 acides aminés (un peptide de 80 acides aminés aura environ une masse moléculaire de 80×110/1000 = 8,8 kDa).
On distingue généralement plusieurs classes de HSPs, nommées ainsi d’après leur masse moléculaire Hsp100 ; Hsp90 ; Hsp70 ; Hsp60 ; Hsp40 ; Hsp de 20 à 30 kDa et Hsp10.
Rôle et mécanismes d’action des HSPs
Rôle général des HSPs
Les HSPs agissent comme des chaperons moléculaires dont les principales fonctions peuvent se résumer ainsi :
- Conformation spatiale des protéines nouvellement synthétisées.
- Prévention de l’agrégation des protéines mal repliées.
- Re conformation des protéines endommagées.
- Neutralisation des protéines irréversiblement endommagées pour les dégrader (via le système ubiquitine-protéasome) ou les amener à l’autophagie
Transport des fragments de protéines nouvellement synthétisés
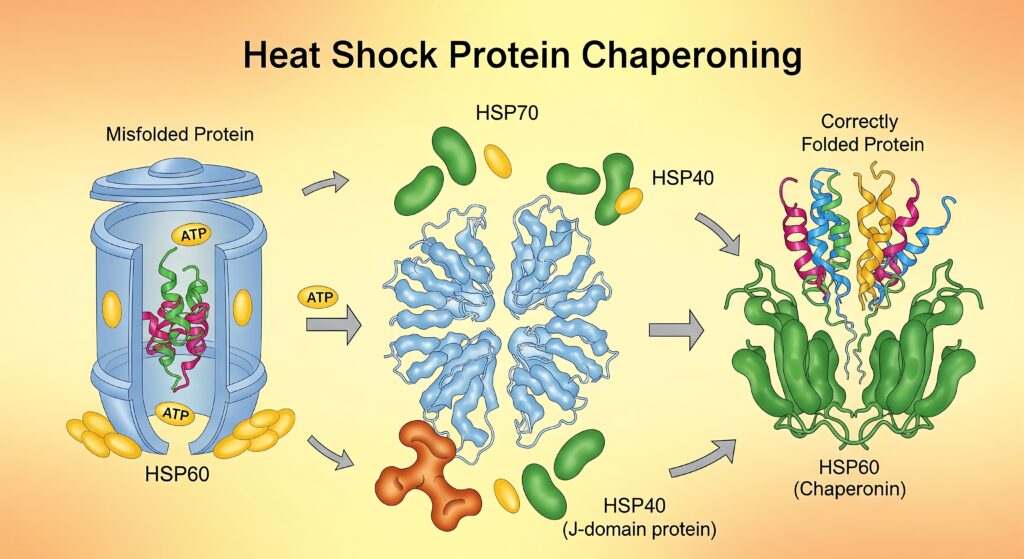
En résumé, les HSP ont besoin d’énergie pour fonctionner.
Les HSPs entre résilience et énergie
Les HSPs protègent et réparent les protéines, préservant ainsi l’efficacité cellulaire. Elles maintiennent la fonction mitochondriale, permettant une récupération plus rapide de l’ATP. Leur activité contribue à une récupération physique plus rapide, à une réduction de la fatigue et à un meilleur bien-être général
Les HSPs en tant que protecteurs cellulaires
Les HSPs maintiennent l’homéostasie protéique (protéostasie), qui garantit que les protéines cellulaires sont correctement repliées et fonctionnelles. Sous l’effet du stress, tel que la chaleur dégagée par l’exercice physique, l’exposition à la chaleur ou au froid extérieur ou le stress oxydatif, les protéines peuvent être endommagées ou mal repliées. Les HSPs empêchent ces protéines endommagées de s’agréger et aident à les réparer ou à les éliminer.
En protégeant le mécanisme cellulaire, les HSPs préservent l’efficacité énergétique. Les protéines mal repliées peuvent perturber le métabolisme cellulaire, obligeant les cellules à « travailler plus dur » et à consommer plus d’ATP. Les HSPs réduisent cette demande énergétique supplémentaire.
Les HSPs et la récupération énergétique
Pendant la récupération après un stress (par exemple, après une activité physique intense), les cellules subissent une déplétion temporaire en ATP et un stress oxydatif. Les HSPs aident à replier les enzymes endommagées et à stabiliser les protéines mitochondriales, qui sont essentielles à la production d’ATP. En maintenant la fonction mitochondriale, les HSPs favorisent une restauration plus rapide de l’énergie, aidant ainsi les tissus à se rétablir plus efficacement. Rappelons ici que le signal de l’apoptose est donné par les mitochondries.
Les HSPs et le bien-être systémique
En plus d’assurer la protection des protéines contre les dommages liés au stress cellulaire, les HSPs soutiennent aussi directement le système immunitaire en favorisant le repliement correct des anticorps. Ce rôle de chaperon garantit que seules des immunoglobulines fonctionnelles sont produites, capables de défendre efficacement l’organisme contre les agents pathogènes. Ainsi, en influençant à la fois la fonction immunitaire et la résilience cellulaire, les HSPs contribuent au maintien des niveaux d’énergie et de la santé générale. Le stress chronique ou le vieillissement peuvent réduire l’expression des HSPs, entraînant une agrégation des protéines, un dysfonctionnement mitochondrial et de la fatigue.

Le rôle des HSPs chez les plantes
Les HSPs sont des protéines hautement conservées et essentielles. Elles constituent donc une famille universelle de protéines présentes dans pratiquement chez tous les organismes vivants, des bactéries, aux plantes et aux humains.
Chez les plantes, les HSPs jouent un rôle crucial dans la tolérance aux conditions défavorables, notamment la chaleur et la sécheresse. Elles seules permettent aux cellules végétales de maintenir leurs fonctions vitales dans des milieux hostiles.
Le figuier de barbarie (Opuntia ficus-indica), plante emblématique des régions sèches et semi-désertiques, et notamment son fruit la figue de barbarie, illustrent bien cette adaptation. En effet, c’est pendant la saison la plus chaude et aride que le fruit de cette plante murie, mobilisant ainsi un arsenal de protéines de choc thermique, notamment les HSP70, pour protéger ses protéines structurales et enzymatiques. Ces protéines contribuent à la stabilité des membranes cellulaires, à la protection de l’appareil photosynthétique et à la survie de la plante lors de périodes de sécheresse prolongée.
Pour une meilleure compétition au sein d’un biotope chaud, sec et radiatif, les Opuntia (comme toutes les plantes à métabolisme CAM (métabolisme acide crassulacéen) ont répliqué les gènes des HSF et des HSP par polygénie et pour certaines espèces par polyploïdie. Le nombre de gènes fonctionnels est ainsi directement associée à la quantité de motif moléculaire promoteur et répresseur de ces gènes. TEX-OE®, l’extrait de Figue de Barbarie, utilise mes motifs moléculaires donnant un avantage compétiteur de la plante pour une meilleures récupération et restauration.
Les HSPs occupent ainsi une place centrale dans la résilience de la figue de Barbarie, dont les extraits de cladodes, de fleurs, et surtout de fruits, sont riches en composés bioactifs tels que les flavonoïdes, polyphénols, et pigments comme les bétalaïnes. Agissant en synergie avec l’effet protecteur des HSPs, ces composés renforcent la résistance de la plante au stress oxydatif.
Références scientifiques
Ces sujets vous intéressent ?
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité
Épigénétique : le chef d’orchestre de vos gènes
Temps de lecture : 7 minutes
Épigénétique : l’étude des changements dans la fonction des gènes sans altération de la séquence de l’ADN
L’étude des changements dans la fonction des gènes ayant lieu sans altération de la séquence de l’ADN » constitue l’épigénétique. Ce terme fut introduit pour la première fois en 1942 par Waddington.
L’épigénétique est aussi le mécanisme qui met en musique la lecture des gènes portés par notre ADN. Autrement dit, c’est le mécanisme qui régule l’expression de nos gènes. Tel un chef d’orchestre qui dirige ses musiciens, l’épigénétique régule l’activité des gènes en fonction de l’environnement soit en les activant soit en les inhibant. Quand un gène est activé, on dit qu’il s’exprime, quand il ne s’exprime pas on dit qu’il est réprimé. Le mot « épigénétique » est une métonymie.
Cellules, gènes et protéines : rappels
Notre corps est composé d’organes qui jouent une rôle grâce à des tissus organisés avec des cellules spécialisées. La cellule est donc la plus petite unité fonctionnelle de notre organisme . Elles sont composées d’un noyau et d’un « cytoplasme » limités par des membranes et dans lesquelles baignent des unités fonctionnelles appelées organites. L’existence même de la cellule repose sur des protéines , suite d’acides aminés dans un ordre et une organisation spatiale définis pour leurs fonctions.
Un gène est un segment d’une grosse molécule appelée ADN consignant sous la forme d’un code « code génétique », la séquence précise des acides aminés codant les protéines de structures comme les collagènes et fonctionnelles comme les enzymes.
Exemples de régulation : adaptative et épigénétique
- Modulation adaptative de l’expression d’un gène.
Le fait de consommer du glucose (sucre d’origine végétal) provoque chez l’humain la production de d’insuline hormone indispensable pour faire pénétrer le glucose dans la cellule. L’insuline est une protéine encodée dans l’ADN (51 acides aminés) du chromosomes 11. L’on conçoit bien que nous synthétisons l’insuline lorsque la molécule de glucose apparaît dans le sang : c’est l’activation du gène. Cette synthèse s’arrête quand le glucose est en dessous d’une concentration minimale. L’apparition du glucose dans le sang (glycémie) a provoqué l’activation du gène codant l’insuline. La normalisation adaptative du taux d’insuline relève de la régulation post-transcriptionnelle et post-traductionnelle . - Régulation fonctionnelle épigénétique de l’expression d’un gène.
A côté de ces mécanismes de régulation de l’’expression du gène de l’insuline, il existe une régulation épigénétique induite par les adipocytes. Les cellules graisseuses envoient un message négatif sur la production de l’insuline en raison du stockage excessif de réserve. Ce message provoque une baisse de la production d’insuline pour ralentir le stockage. Ce mécanisme épigénétique, ne modifie pas l’ADN et persister de manière transgénérationnelle ou somatique comme chez les personnes âgées. Ainsi, l’espèce humaine peut d’adapter à des périodes de disette où il existe un nécessité de faire des réserves. Cela permet aussi d’ajuster le taux d’insuline lorsque la régulation adaptative est moins efficace. Ces transformations épigénétiques sont réversibles id3. Le point clef de la réversibilité repose principalement sur l’acétylation/désacétylation des histones .
Il existe des transformations épigénétiques irréversibles pour l’individu sans modification de l’ADN. L’exemple des abeilles montre que l’épigénétique peut affecter de manière irréversible la totalité d’un individu et sa destinée. Le génome des abeilles d’une ruche provient d’une source identique puisque issu d’une seule fécondation d’une reine. L’alimentation (gelée royale) permettra l’expression des gènes caractérisant la reine et réprimant la transformation en mâle. Chez ces insectes, le facteur permettant la sélection femelle/mâle est mis en place par la communauté des hyménoptères . Une fois établis, les caractères sexuels (phénotype) indispensables au renouvellement de l’essaim sont irréversible.
Accessibilité des gènes et rôle des histones
Pour qu’un gène soit activé, il doit pouvoir être lu tout comme une partition de musique. Le rôle de l’épigénétique est donc de réguler l’accessibilité des gènes en jouant sur l’enroulement de l’ADN autour des histones.
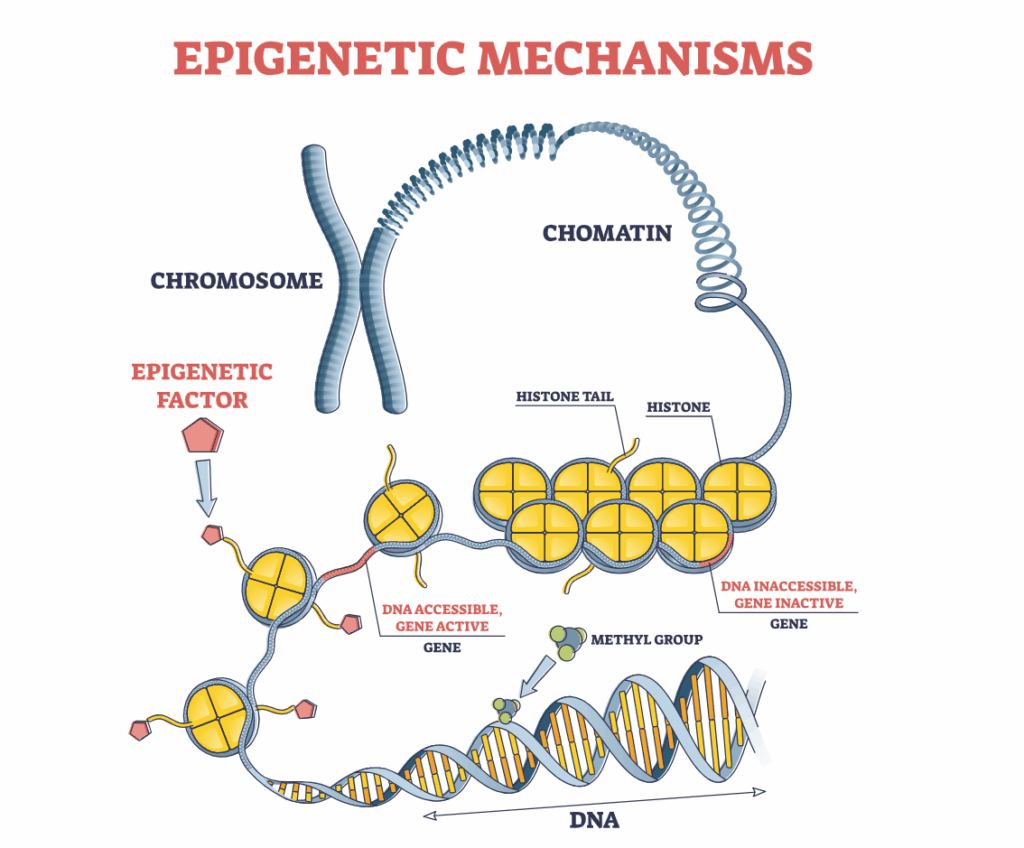
Mécanismes épigénétiques
Les 3 principaux mécanismes épigénétiques
1. La méthylation de l’ADN : ajout d’un groupe méthyle sur certaines bases de l’ADN, ce qui peut « éteindre » un gène. Cette modification peut être réversible bien qu’elle modifie chimiquement l’ADN sans en altérer la séquence. Ces modifications ne sont pas transgénérationnelles.
2. Les modifications des histones : les histones sont des protéines comme des cabestans, autour desquelles l’ADN s’enroule; leur modification influence la compaction de l’ADN et donc l’accès aux gènes. Il existe quatre types majeurs de modifications adaptatives des histones: l’acétylation, la méthylation, la phosphorylation et l’ubiquitinylation.
3. Les ARN non codants : ils peuvent interagir avec l’ADN ou l’ARN pour réguler l’expression génétique.
Génome, chromosomes et expression différentielle
L’ADN (ou acide désoxyribonucléique) est une molécule constituée d’une succession d’environ 3 milliards de bases dites azotées, qui, mesurerait près de 2 mètres de long si on la déroulait. Il existe 4 sortes de bases azotées : A pour adénine, T pour thymine, G pour guanine et C pour cytosine où chaque individu possède une suite de bases unique. Ce code unique de l’information génétique d’une personne constitue son génome.
Les gènes sont des portions de l’ADN ayant une fonction bien définie. Ils sont lus par des enzymes pour permettre la fabrication de protéines, des molécules qui constituent et font fonctionner tout organisme vivant.
On retrouve cette grande molécule d’ADN dans les chromosomes organisés en paires dans le noyau des cellules. Chez l’être humain, on compte 23 paires de chromosomes contenues dans le noyau de chaque cellule de notre corps. Ainsi, l’ensemble de nos cellules contient la même molécule d’ADN. Pourtant, pour faire un corps fonctionnel, il faut des types de cellules différents : des cellules de cœur, des cellules de peau, des neurones,… C’est donc là qu’intervient l’épigénétique en régulant l’expression de nos gènes. Si toutes les cellules contiennent le même génome, toutes n’expriment pas pour autant les mêmes gènes.
Dérèglements épigénétiques
Comme toute machinerie, elle peut parfois se dérégler. Notre environnement et notre hygiène de vie peuvent influencer le fonctionnement de nos marques épigénétiques. Le dérèglement de l’épigénétique désigne un déséquilibre ou une altération des mécanismes épigénétiques qui régulent l’expression des gènes sans modifier la séquence de l’ADN. Ces dérèglements peuvent perturber le fonctionnement normal des cellules et sont souvent associés à des maladies comme le cancer, certaines maladies neurodégénératives, des troubles métaboliques ou encore des maladies auto-immunes.
Exemples de dérèglement
4 Exemples de Dérèglement épigénétique
1. Un dérèglement épigénétique peut survenir lors d’une Hyperméthylation anormale des gènes suppresseurs de tumeurs. Les gènes suppresseurs de tumeurs (comme p53, BRCA1, etc.) ont un rôle crucial : ils empêchent la multiplication incontrôlée des cellules. En temps normal, ces gènes sont actifs : ils freinent la division cellulaire, réparent l’ADN ou déclenchent la mort de cellules anormales. Lors d’un dérèglement épigénétique, certains de ces gènes peuvent subir une hyperméthylation (ajout excessif de groupes méthyles sur leur ADN, surtout dans les régions promotrices). Cette hyperméthylation « éteint » leur expression, ce qui désactive leur fonction protectrice. Ainsi, les cellules peuvent se diviser sans contrôle et entraîner le développement de tumémeurs.
2. Hypométhylation globale de l’ADN. En situation normale, certaines parties de l’ADN, notamment les séquences répétitives ou inutiles, sont fortement méthylées pour rester silencieuses. En cas de hypométhylation globale (manque général de méthylation dans le génome), ces régions peuvent devenir actives alors qu’elles ne devraient pas l’être et entraîner :
- L’activation de séquences rétrovirales internes (inactives d’habitude).
- La réactivation de gènes oncogéniques (favorisant la croissance cellulaire).
- Une instabilité chromosomique (erreurs de duplication ou de réparation de l’ADN).
Altérations des histones. L’ADN est enroulé autour de protéines appelées histones, formant un complexe appelé chromatine. Ces histones peuvent subir des modifications chimiques (acétylation, méthylation, phosphorylation, etc.). Ces modifications influencent la structure de la chromatine :
- Chromatine ouverte (euchromatine) → gènes actifs (facilement transcrits).
- Chromatine fermée (hétérochromatine) → gènes inactifs (inaccessibles).
Un dérèglement de ces modifications peut donc 1/activer des gènes qui ne devraient pas l’être et 2/ Réprimer des gènes essentiels (comme les gènes de réparation de l’ADN).
4. Perturbations dans les ARN non codants. Les ARN non codants (comme les microARN ou les longs ARN non codants) ne produisent pas de protéines, mais régulent l’expression des gènes. Les microARN par exemple peuvent bloquer la traduction d’un ARN messager ou le dégrader. Si ces ARN sont surrégulés ou sous-régulés :
- Des protéines essentielles peuvent être bloquées.
- Des oncogènes peuvent ne plus être contrôlés.
Ces types de dérèglement sont impliqués dans de nombreux cancers et maladies neurodégénératives.
Pour un exemple détaillé voir à la fin du document
Faits fascinants
3 faits fascinants sur l’épigénétique
1. “Vous êtes ce que votre père mange”
Il est bien établi que les femmes enceintes doivent consommer des quantités suffisantes de folate (également appelé acide folique ou vitamine B9) afin de réduire les risques de fausses couches et de malformations congénitales. Ce nutriment joue un rôle essentiel dans le processus de méthylation de l’ADN, un mécanisme qui régule l’expression normale des gènes.
Pour la première fois, des chercheurs de l’Université McGill à Montréal (Québec, Canada) ont démontré que cet aspect de l’alimentation ne concerne pas uniquement la mère. En effet, ils ont découvert que l’apport en folate chez le père peut également influencer la santé et le développement de l’enfant à naître.
(https://www.nature.com/articles/ncomms3889)
2. “L’exercice physique affecte l’épigénétique”
L’exercice physique induit des schémas de méthylation différents dans les gènes associés à la régulation du métabolisme cellulaire des glucides et au remodelage structurel, ce qui a suggéré aux chercheurs d’une étude de 2014 que les changements transcriptionnels dans le muscle squelettique dus à l’exercice physique sont liés aux changements de méthylation de l’ADN.
(https://www.tandfonline.com/doi/full/10.4161/15592294.2014.982445)
3. « Il existe une horloge épigénétique »
L’analyse d’une grande variété d’échantillons de tissus prélevés sur un grand nombre de personnes (13 000) d’âges différents a révélé une évolution de l’ADN méthylé en corrélation avec l’âge. L’horloge épigénétique (ou epigenetic clock en anglais) se définit comme un outil biologique qui permet d’estimer l’âge biologique d’un individu, en se basant sur les modifications épigénétiques de son ADN, notamment la méthylation de l’ADN.
(https://www.nature.com/articles/508168a)
Plus en détail — Exemple
PLUS EN DETAIL – Un exemple d’Epigénétique
L’exemple le plus illustratif des modifications épigénétiques est celui de la différenciation cellulaire. Ainsi, au cours de la morphogenèse, une seule cellule diploïde (œuf fertilisé ou zygote) va se diviser en plusieurs cellules qui à leur tour vont se différencier en plusieurs types cellulaires comme les neurones, les cellules musculaires, les cellules cardiovasculaires etc. et ceci en activant certains gènes et en inhibant d’autres.
Le remodelage de la chromatine est considéré comme le facteur épigénétique majeur responsable de la régulation de l’expression génique sans altération des séquences d’ADN. La chromatine est un complexe formé de chaines d’ADN enroulées sur des sphères protéiques (histone). Il est donc évident que si cette association entre l’ADN et l’histone change ; l’expression génique change aussi. Ce remodelage de la chromatine est effectué via 2 mécanismes essentiels :
1- Les modifications pst-traductionnelles des protéines de l’histone comme l’acétylation et la méthylation des acides aminés.
2- La méthylation de l’ADN et notamment de la cytosine en 5-méthylcytosine à l’aide de DNA méthyltransférase (DNMT-1). Ainsi, certaines zones le long de la chaine nucléotidique montrent un degré de méthylation plus élevé que d’autres. Il est à noter que les gènes hyperméthylés sont moins transcrits que les gènes pas ou légèrement méthylés.
Suivant les zones de la chromatine où les modifications épigénétiques sont opérées, les gènes situés à ce niveau seront plus ou moins activés selon le type du mécanisme épigénétique [(dé)méthylation et/ou (dés) acétylation] mis en œuvre. Ainsi la désacétylation de l’histone et la méthylation de l’ADN vont doter la chromatine d’une structure plus compacte moins accessible à l’enzyme de transcription ; RNA polymérase avec comme conséquences l’arrêt ou le ralentissement de l’expression génique. En revanche, l’acétylation de l’histone et la déméthylation de l’ADN contribuent à desserrer les liens entre l’ADN et l’histone facilitant l’accès à l’enzyme de transcription.
Il est donc clair que les facteurs épigénétiques sont des facteurs clé pouvant jouer un rôle décisif dans l’orientation de l’activité d’une cellule (différenciation et transformation) en favorisant ou en inhibant l’expression de certains gènes déterminant ainsi son phénotype. Il est à noter que la méthylation de l’ADN est un processus essentiel au cours du développement embryonnaire et dans les cellules somatiques car il permet de réguler l’expression génique d’une manière temporellement et spatialement-dépendant. Cependant, des schémas aberrants de (dé)méthylation d’ADN sont associés à des malignités humaines en comparaison avec des tissus normaux et notamment dans les zones où sont localisés les gènes suppresseurs de tumeurs. L’hyperméthylation de ces zones a pour effet d’inhiber l’expression de ces gènes et notamment p53.
Références
- L’épigénétique, quand vos gènes s’expriment.
- Épigénétique : qu’est-ce que c’est ?
- Régulation post-transcriptionnelle : mécanisme gérant la transcription de l’ADN d’un gène en ARN messager & Régulation post-traductionnelle : mécanisme gérant la traduction du ARNm en protéine.
- Le code épigénétique des histones.
- L’Abeille et l’épigénétique.
- Le code épigénétique des histones.
Ces articles pourraient vous intéresser

Ces sujets vous intéressent ?
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité
Quelle est la différence entre la vitamine K1 et K2?
Quelle est la différence entre la vitamine K1 et K2 ?
La vitamine K est une vitamine liposoluble essentielle à divers processus biologiques, notamment la coagulation sanguine, le métabolisme osseux et articulaire et la santé cardiovasculaire. La vitamine K est essentielle aux communications entre les cellules nerveuses. Les vitamines K1 (Phylloquinone) et K2 (Ménaquinone) contribuent au maintien d’une fonction cognitive optimale, au maintien des capacités de notre cerveau à être en interaction avec notre environnement (concentration, perception, raisonnement, mémoire…). La vitamine K a un rôle fondamental dans la production sphingolipides. L’altération du métabolisme des phospholipides est associée à la détérioration du cerveau et de la mémoire Des niveaux élevés de vitamine K réduisent l’inflammation et le stress oxydatif dans le cerveau, caractéristiques de la neurodégénérescence.
Elle existe principalement sous deux formes : la vitamine K1 (phylloquinone) et la vitamine K2 (ménaquinones). Bien qu’elles partagent une structure chimique de base et certaines fonctions biologiques, ces deux formes diffèrent significativement par leur origine, biodisponibilité, distribution tissulaire et rôle physiologique.
La vitamine K a été identifiée en 1929 pour son rôle dans la coagulation sanguine (le « K » provenant de « Koagulation » en allemand). Elle regroupe un ensemble de composés liposolubles, tous caractérisés par un noyau naphtoquinone, mais différenciés par leurs chaînes latérales. Les deux formes les plus étudiées sont la phylloquinone (vitamine K1) et les ménaquinones (vitamine K2), dont il existe plusieurs sous-types (MK-4 à MK-13).
Au total il existe au moins une douzaine de formes naturelles de la vitamine K, mais seules les K1, MK-4 et MK-7 sont couramment étudiées et utilisées en santé humaine.
La vitamine K1
La vitamine K1 est dotée d’une chaîne latérale phytyl. Elle est principalement présente dans les légumes à feuilles vertes (persil, épinards, brocoli, chou frisé, etc.) mais aussi chez les phéophycées (Padines). La teneur en phylloquinone dans les algues et leurs extraits varient en fonction de l’espèce d’algue mais aussi du procédé d’extraction. En général, les algues brunes (phéophycées), comme le kelp (Laminaria japonica), contiennent des quantités relativement élevées de vitamine K1 (jusqu’à 66 µg de phylloquinone pour 100 g) tandis que d’autres produits d’aquaculture, comme la spiruline (cyanobactéries), en contiennent moins (environ 25,5 µg pour 100 g).
Bon à savoir! Un comprimé de DICTYOLONE®K comprend naturellement en moyenne 1μg de phylloquinone provenant de l’extrait de Padina sp. EPP® mais peut varier et a donc été ajusté à 11,25μg afin d’assurer une dose quotidienne constante et de s’affranchir des variations naturelles. L’Union Européenne recommande un apport quotidien de 75 μg de vitamine K. (Règlement (UE) no 1169/2011).
Etant ici précisé que les traitements avec des antivitamine K (AVK) supposent un apport alimentaire respectant cet apport quotidien.
La vitamine K1 est dotée d’une chaîne latérale phytyl. Elle est principalement présente dans les légumes à feuilles vertes (épinards, brocoli, chou frisé, etc.) mais aussi dans les algues telles que les Padines. La teneur en phylloquinone dans les algues et leurs extraits varient en fonction de l’espèce d’algue mais aussi du procédé d’extraction. En général, les algues brunes, comme le kelp (Laminaria japonica), contiennent des quantités relativement élevées de vitamine K1 (jusqu’à 66 µg de phylloquinone pour 100 g) tandis que d’autres types d’algues, comme la spiruline, en contiennent moins (environ 25,5 µg pour 100 g).
La vitamine K1 est absorbée principalement dans l’intestin grêle, mais sa biodisponibilité est limitée, surtout lorsqu’elle est consommée sans matières grasses. Elle est majoritairement concentrée dans le foie, où elle participe à la synthèse des facteurs de coagulation. La vitamine K1 participe principalement à la coagulation du sang en activant les protéines de la coagulation (facteurs II, VII, IX, X), permettant donc leur carboxylation γ-glutamique, un processus qui les rend fonctionnelles.
La vitamine K1 joue également un rôle important dans la santé osseuse et le maintien de la densité minérale osseuse. La vitamine K1 est un cofacteur de la γ-glutamyl carboxylase, une enzyme qui permet la carboxylation de certaines protéines osseuses, en particulier l’ostéocalcine, protéine synthétisée par les ostéoblastes (cellules qui construisent l’os). Une fois carboxylée (activée grâce à la vitamine K1), l’ostéocalcine peut lier le calcium et l’incorporer efficacement dans la matrice osseuse. Des études épidémiologiques ont montré que des apports plus élevés en vitamine K1 sont associés à :
- Une meilleure densité minérale osseuse (DMO), surtout chez les femmes ménopausées.
- Une réduction du risque de fractures
Bien que la vitamine K1 est principalement connue pour son rôle dans la coagulation sanguine, elle participe aussi à la santé osseuse via l’activation de protéines essentielles à la minéralisation comme l’ostéocalcine. Une carence en vitamine K1 peut contribuer à une diminution de la qualité osseuse sur le long terme même si elle est moins efficace que la vitamine K2, en raison de sa biodistribution plus restreinte.
La Vitamine K2
La vitamine K2, contrairement à la vitamine K1, regroupe les ménaquinones (MK-n), dont la chaîne latérale est formée de résidus isoprénoïdes. Le nombre « n » indique le nombre d’unités isopréniques (par ex. MK-7, MK-9). Ces variations influencent leur demi-vie, biodisponibilité et distribution tissulaire. Elles sont présentes dans les aliments fermentés (notamment le natto, riche en MK-7), les produits d’origine animale (jaune d’œuf, foie), et certains fromages vieillis.
La vitamine K2, particulièrement MK-7 et MK-9, possède une demi-vie plus longue (jusqu’à 72 heures pour le MK-7) et une meilleure distribution extra-hépatique, notamment vers les os, articulations et les parois artérielles. La vitamine K2 active l’ostéocalcine, une protéine qui fixe le calcium dans la matrice osseuse. Une carence en K2 peut donc entraîner une minéralisation insuffisante, augmentant le risque d’ostéoporose.
La vitamine K2 MK-7 et notamment MenaQ7® a été cliniquement testée dans le traitement de la polyarthrite rhumatoïde où les ménaquinones (MK) induisent l’apoptose des cellules synoviales lors de la polyarthrite rhumatoïde (PR).
La vitamine k2 à beaucoup moins d’incidence sur la coagulation que la vitamine K1. Une étude de 2021, indique qu’une supplémentation en MK-7 à la dose recommandée n’affecte pas l’activité de coagulation des facteurs de coagulation dépendants de la vitamine K et n’augmente pas la carboxylation de la prothrombine chez les individus en bonne santé. Cela indique que l’administration de MK-7 ne modifie pas l’équilibre hémostatique chez les populations saines sans traitement anticoagulant.
Dans cette étude, quarante volontaires sains âgés de 25 à 40 ans ont été recrutés. La ménaquinone-7 (MK-7) a été administrée à raison de 90 μg pendant 30 jours. Le temps de prothrombine (TP), le temps de céphaline activé (TCA), le temps de thrombine (TT), les activités des facteurs de coagulation II, VII, IX et X et la protéine induite par l’absence de vitamine K ou l’antagoniste-II (PIVKA-II) ont été mesurés les jours 0 et 30 après l’administration de MK-7.
Le saviez-vous?
Il existe aussi une forme synthétique la Vitamine K3 (Ménadione) mais elle est non naturelle et toxique à haute dose et donc interdite à la consommation humaine dans la plupart des pays.
Références scientifiques
- Alisi L et al. 2019. The Relationships Between Vitamin K and Cognition: A Review of Current Evidence. Front Neurol. 2019 Mar 19;10:239. doi: 10.3389/fneur.2019.00239. PMID: 30949117; PMCID: PMC6436180.
- Alonso N et al. 2023. Role of Vitamin K in Bone and Muscle Metabolism. Calcif Tissue Int. 2023 Feb;112(2):178-196. et al. The role of menaquinones (vitamin K2) in human health. Br J Nutr. 2013.
- Booth SL et al. Dietary phylloquinone intake and bone mineral density in men and women. Am J Clin Nutr. 80(2): 715–720. 2004.
- Booth SL et al. Effect of vitamin K supplementation on bone loss in elderly men and women. Am J Clin Nutr. 87(5): 1420–1427. 2008
- Booth SL, Shea MK, Barger K, et al. Association of vitamin K with cognitive decline and neuropathology in community-dwelling older persons. Alzheimer’s Dement. 2022; 8:e12255.
- Carence en vitamine K.
- Gast GCM et al. A high menaquinone intake reduces the incidence of coronary heart disease. J Nutr. 2009.
- Hariri . et al. 2021. Vitamin K2-a neglected player in cardiovascular health: a narrative review. Open Heart. 2021 Nov;8(2):e001715. doi: 10.1136/openhrt-2021-001715.
- Hao G et al. Higher dietary vitamin K intake is associated with a lower risk of hip fracture in women. Osteoporos Int. 26(3): 1235–1243. 2015
- Iwamoto J et al. Low serum vitamin K1 levels and vertebral fractures in Japanese women. J Bone Miner Metab. 26(1): 41–47.2008
- Ren R., Liu J., Cheng G., Tan J. Vitamin K2 (Menaquinone-7) supplementation does not affect vitamin K-dependent coagulation factors activity in healthy individuals
- Shearer MJ, Newman P. Metabolism and cell biology of vitamin K. Thromb Haemost. 2008.
- Vitamine K et fonctions cognitives chez la personne âgée en santé : une approche épidémiologique nutritionnelle.
Ces sujets vous intéressent ?
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité
Compatibilité Phylogénique : Quand l’Évolution Végétale Inspire la Santé Humaine
Temps de lecture : 4 minutes
La Compatibilité Phylogénique : Quand l’Évolution Végétale Inspire la Santé Humaine
Introduction : Les Liens Invisibles entre les Règnes du Vivant
Saviez-vous que derrière l’apparente diversité du monde vivant se cachent des similitudes profondes ? L’évolution a tissé des liens complexes entre les règnes animal et végétal, partageant des mécanismes biologiques fondamentaux. Cet article explore le concept fascinant de la compatibilité phylogénique et son potentiel révolutionnaire pour la santé humaine.
Qu’est-ce que la Compatibilité Phylogénique ? Un Héritage Évolutif Partagé
Au fil de l’évolution, de nombreux processus métaboliques sont devenus communs aux règnes animal et végétal. Ces mécanismes sont codés dans ce que l’on appelle les gènes cladistiques. Ces gènes sont hérités d’un ancêtre commun et se retrouvent chez toutes les espèces partageant cette origine. Pensez aux canaux à eau, aux protéines de stress thermique ou aux enzymes clés du métabolisme des sucres (comme le cycle de Krebs) : ils sont étonnamment similaires, voire identiques, chez une vaste majorité des organismes vivants. L’ancêtre commun, à l’aube de la vie sur Terre, a inscrit ces gènes essentiels dans notre patrimoine génétique commun.
Cette parenté évolutive se manifeste également dans l’expression de caractéristiques morphologiques, qu’elles soient définitives ou temporaires (grâce aux gènes plésiomorphes). Un exemple frappant est le développement embryonnaire humain, qui reproduit des formes observées chez nos ancêtres évolutifs. C’est l’idée maîtresse de la théorie de la récapitulation de Haeckel, souvent résumée par l’adage « l’ontogénèse récapitule la phylogénèse ».
En substance, les gènes cladistiques sont des outils biologiques fondamentaux, hérités et conservés par tous les descendants d’un même ancêtre. Ils fonctionnent grâce à des mécanismes de régulation précis (« activation et répression ») qui assurent leur mise en œuvre adéquate.
La Compatibilité Phylogénique au Service de la Santé : Une Nouvelle Voie Thérapeutique
Fort de cette compréhension des similitudes métaboliques entre les règnes animal et végétal, il devient possible d’envisager une approche thérapeutique innovante. Des substances naturelles issues de plantes alimentaires pourraient être mises à disposition des professionnels de santé pour offrir des soins performants et ciblés. Ces recherches sont guidées par la similarité de nos métabolismes, un héritage direct de notre histoire évolutive commune. Ainsi, les molécules thérapeutiques extraites de végétaux peuvent agir pour restaurer des fonctions métaboliques altérées chez l’humain.
Des Cascades Métaboliques Végétales Étonnamment Similaires aux Nôtres
Le monde végétal recèle des cascades métaboliques qui présentent des analogies frappantes avec celles des humains. Cette similarité suggère que les gènes codant les enzymes et les protéines impliquées dans ces processus sont étonnamment proches entre les plantes et les humains. Plus fascinant encore, les mécanismes de régulation de ces gènes sont souvent semblables dans les deux règnes.
Les Régulateurs Végétaux : Des Alliés Naturels pour Restaurer nos Fonctions
Les régulateurs issus du règne végétal peuvent intervenir de manière similaire à ceux du monde animal et humain. C’est cette compatibilité qui ouvre la voie à des thérapies ciblées. Ils pourraient potentiellement restaurer une fonction déficiente chez l’humain en agissant sur des dérégulations post-transcriptionnelles ou post-traductionnelles. Cette approche scientifique, ancrée dans la phylogénèse, permet d’identifier et d’isoler des principes actifs de manière rationnelle et prometteuse.
Au-delà des Gènes Cladistiques : Les Fascinants « Gènes Improbables »
Si les gènes cladistiques témoignent d’un héritage commun, la science a également mis en lumière l’existence de « gènes improbables ». Le séquençage du génome de la Padine (Padina pavonica) en 2017 et sa comparaison avec le génome humain a révélé l’intérêt de ces gènes surprenants, présents chez certains végétaux.
Qualifiés d' »improbables » en référence à la théorie du hasard et de la nécessité de Jacques Monod, ces gènes ne semblent pas avoir de fonction essentielle pour la plante elle-même. Ils sont retrouvés sporadiquement chez quelques espèces végétales, indépendamment de leur lignée évolutive.
Certains végétaux peuvent en contenir quelques dizaines, caractérisés par une homologie remarquablement élevée (supérieure à 98%). Contrairement aux gènes cladistiques, ils ne suivent pas les voies de l’évolution humaine. Pourtant, tout comme les gènes hérités, ils sont accompagnés de l’ensemble de la machinerie de régulation nécessaire à leur expression. L’exemple de l’hémoglobine retrouvée chez les fabacées sous forme de léghémoglobine (légumineuse-hémoglobine), avec une similitude frappante, illustre cette fascinante découverte.
Conclusion : Un Nouveau Champ d’Exploration Thérapeutique
La compatibilité phylogénique, qu’elle se manifeste à travers les gènes hérités ou les surprenants « gènes improbables », ouvre un champ d’exploration thérapeutique passionnant. Comprendre et exploiter les similitudes fondamentales entre les règnes animal et végétal pourrait révolutionner notre approche de la santé et du bien-être, en nous offrant des solutions naturelles, innovantes et profondément ancrées dans l’histoire de la vie sur Terre.
Ces sujets vous intéressent ?
Recevez chaque mois notre Newsletter pour ne pas manquer notre actualité
Ces articles pourraient vous intéresser

Cellule & Virus : Une Coopération Ancestrale Révélée
La vie d'une cellule
Transcription de la vidéo:
Cellules & Virus : Une Coopération Ancestrale Moteur de l’Évolution
Depuis peu, la science nous a ouvert le spectacle du monde intérieur de la cellule. Ce monde est le théâtre, entre autre, d’une coopération ancestrale entre les cellules et les virus. Cette coopération a été l’un des moteurs les plus puissants de l’évolution des êtres vivants. Chaque cellule vit dans un environnement où coexistent d’autres cellules. Elles sont continuellement en communication les unes avec les autres.
Le Monde Intérieur de la Cellule : Transcription et Traduction
Les instructions codées dans les gènes sont transcrites pour être transportées hors du noyau où elles seront traduites en des milliers de protéines ayant des formes, des conformations et des fonctions différentes.
Les Gardiens de l’Intégrité Cellulaire : Protéines Chaperonnes et Globules Blancs
Les protéines seront inspectées et contrôlées par les gardiens de notre intégrité : les protéines chaperonnes, nos globules blancs, etc.
Ces soldats ubiquitaires vérifient tous les fragments de protéines au moyen de signaux permettant d’identifier ce qui est dangereux ou non, quels sont les dégâts ou l’intérêt, ou ce qui est susceptible d’affecter ou de détourner la machinerie cellulaire.
Notre Coexistence avec les Microbes : Identifier l’Ami et l’Ennemi
Nous vivons avec plus de bactéries et de composés viraux que nous n’avons de cellules. Nous devons donc identifier ce qui est dangereux ou utile face aux protéines qui caractérisent la surface de ces êtres invisibles.
La Peau : Notre Première Ligne de Défense
Notre première frontière est la peau. Elle empêche l’entrée des intrus, hélas parfois des inopportuns peuvent pénétrer et résider dans notre corps.
L’Invasion Virale : Adhésion et Absorption Cellulaire
Les cellules se déplacent d’une cellule hôte à une cellule à infecter. L’adhésion à la membrane cellulaire et l’absorption sont liées à la capacité du virus à lire le récepteur cellulaire adéquate. L’adhésion est la première étape requise pour permettre à un virus d’infecter une cellule. Ce comportement est identique chez la plupart des virus possédant une capside comme le HIV ou les virus de la famille de l’herpès.
Comprendre l’Interaction Hôte-Envahisseur : Vers l’Évolution
L’interprétation de ces étapes d’adhésion et d’absorption est nécessaire pour une pleine compréhension des mécanismes qui lient les envahisseurs à leur hôte cellulaire. De ces échanges entre virus et cellules hôtes, nous pouvons en sortir plus évolués.
Narrateur : Gilles Gutierrez – Fondateur des laboratoires ICP-TEXINFINE et TEXINFINE Tahiti